Biologie du système neuromusculaire (MUSE)
Informations pratiques

Faculté de santé de Créteil
Organigramme de l’équipe
Plan d’accès vers la faculté de santé (campus de Créteil)
Plan d’accès vers l’Ecole nationale vétérinaire d’Alfort (campus de l’EnvA)
Projets scientifiques
Les cellules souches musculaires au premier plan de la myogenèse
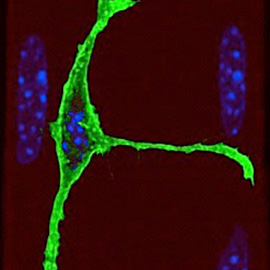
Cellule souche musculaire (MuSC)
Nous nous intéressons depuis longtemps à la compréhension des réseaux de régulation de la myogenèse au cours du développement et chez l’adulte, avec un accent particulier sur les cellules souches musculaires (appelées cellules satellites). Grâce à des cribles à grande échelle, nous avons identifié les signatures transcriptionnelles et épigénétiques caractéristiques de la transition entre quiescence et activation des cellules satellites. Nous étudions plusieurs facteurs et voies qui régulent la quiescence, l’activation, la différenciation, l’autorenouvellement et la signature épigénétique des cellules satellites. En outre, nous étudions la réponse adaptative des cellules satellites aux facteurs stressants de l’environnement. Enfin, nous avons mis au point un nouveau protocole qui permet d’isoler les cellules satellites véritablement quiescentes, en évitant les artefacts d’activation spontanée introduits par les protocoles classiques et déroulons une série d’expériences à haut débit sur cellule unique afin de poursuivre le décryptage des principaux acteurs des réseaux de gènes impliqués dans le contrôle de la quiescence et de l’activation.
L’élucidation des réseaux de gènes qui contrôlent la quiescence et l’activation des cellules satellites est un défi majeur et un prérequis pour comprendre la remarquable capacité de régénération du tissu musculaire.
Informations détaillées sur le site web ou le compte twitter du groupe Relaix.
Interactions des cellules souches avec leur environnement
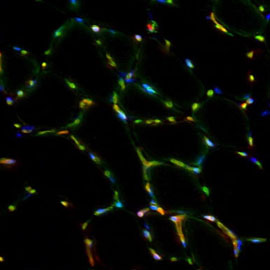
Niche cellulaire de la MuSC
Nous cherchons à décrire comment les cellules souches musculaires sont contrôlées par leur niche, microenvironnement spécialisé qui leur signale un défaut d’homéostasie. Nous nous concentrons sur les cellules périvasculaires (cellules endothéliales, péricytes) et les cellules inflammatoires (en particulier les macrophages) qui influencent la croissance et la régénération musculaires postnatales. Suite à nos découvertes sur la myo-angiogenèse coordonnée, nous cherchons à étudier l’effet de l’hypoxie dans l’orchestration de ces processus. Nos études sur la nature moléculaire de la niche se concentrent sur les facteurs de croissance sécrétés et la matrice extracellulaire. Nous avons récemment dévoilé une cascade Notch/COLV/CALCR qui maintient de façon autonome l’état de repos des cellules satellites.
L’identification des divers facteurs de la niche et de leurs modes d’interaction est une condition préalable à l’utilisation des cellules souches musculaires en médecine régénérative.
Informations détaillées sur le site web, le compte twitter du groupe Relaix ou le site web du groupe Mourikis.
Mécanismes pathogènes et thérapie des troubles neuromusculaires
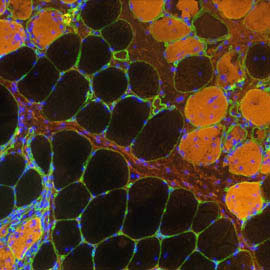
Muscle malade, fibres endommagées
Notre principal objectif biomédical est de comprendre et de traiter les maladies neuromusculaires, notamment la dystrophie musculaire de Duchenne et les myopathies congénitales. Notre capacité à mettre de nouvelles thérapies sur le marché est conditionnée par la qualité des essais précliniques réalisés sur des modèles animaux, prédictifs d’une translation réussie vers les patients humains. Ainsi, un objectif transversal fort pour notre équipe est de caractériser des modèles précliniques spontanés chez le chien domestique et d’établir de nouveaux modèles précliniques de rongeurs. La pertinence de ces modèles est validée par un phénotypage approfondi (histoire naturelle, histologie, évaluation fonctionnelle interdisciplinaire) et le cas échéant, ils sont ciblés par des stratégies thérapeutiques innovantes pharmacologiques ou d’édition du génome.
Les modèles précliniques spontanés et induits constituent un outil précieux pour les étapes exploratoires d’une preuve d’efficacité et d’innocuité avant d’éventuelles applications cliniques chez l’homme.
Informations détaillées sur le site web, le compte twitter du groupe Relaix ou sur le site web des groupes EnvA.
Plasticité, migration et destin des cellules issues de la crête neurale
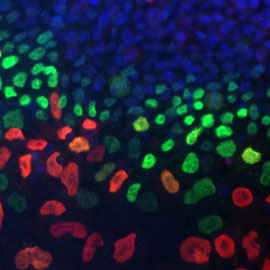
Cellules de crête neurale en migration
Nous développons un programme de recherche multidisciplinaire qui associe génétique moléculaire, biologie cellulaire et mécano-biologie pour comprendre les bases moléculaires et cellulaires du développement des cellules de la crête neurale dans des conditions normales et pathologiques. Les cellules de la crête neurale (CCN) proviennent du neuro-ectoderme de l’embryon précoce de vertébré. Elles passent par une transition épithélio-mésenchymateuse et sont dotées de propriétés souches, prolifératives et migratoires remarquables. Elles contribuent à une multiplicité de types de cellules et fournissent de grands contingents de cellules souches dans les tissus adultes. Nous avons caractérisé le rôle des molécules d’adhésion, de leur interaction avec des facteurs solubles ou de transcription au début de la délamination des CCN et pendant le développement du système nerveux entérique. Nous avons démontré l’importance du couplage entre l’adhésion et la mécanique cellulaire. Nous avons démontré que la voie de signalisation SDF1/CXCR4 régule la ségrégation spatiale des CCN cardiaques à partir des CCN entériques, ainsi que leur chimiotaxie vers le cœur. Nos travaux actuels visent à comprendre comment les CCN s’adaptent aux contraintes métaboliques, mécaniques et biochimiques imposées par leur micro-environnement pour réguler leur plasticité, leur migration et leur différenciation au cours du développement.
La compréhension de la relation entre la biomécanique, le métabolisme énergétique et les facteurs solubles est d’un intérêt crucial pour les cancers, les troubles congénitaux et les thérapies cellulaires.
Les cellules souches dans le développement, la régénération et les maladies du système musculosquelettique
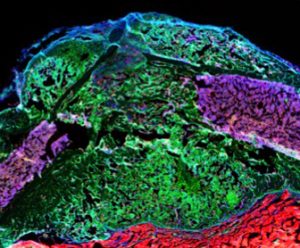
Interaction de cellules souches pendant la régénération osseuse
Notre recherche se concentre sur la biologie des cellules souches squelettiques qui sont à la base des grandes capacités de régénération des tissus squelettiques et qui sont potentiellement déficientes dans diverses maladies et troubles musculosquelettiques. Nous visons à élucider les fonctions des cellules souches dans leur environnement tissulaire complexe, au cours du développement, de la réparation et dans les maladies osseuses. A ces fins, nous utilisons des modèles génétiques de souris, des approches cellulaires et les outils de la génomique. Nous nous concentrons en particulier sur le périoste, le tissu recouvrant la surface externe de l’os et sur le muscle squelettique adjacent à l’os, qui joue aussi un rôle essentiel dans la régénération osseuse.
Plus d’informations sur ce thème sur le site web du groupe Colnot.
Publications récentes
=> télécharger une liste complète des articles publiés par les membres de l'équipe
Mise à jour en mars 2021*** CI-DESSOUS, UNE SELECTION D'ARTICLES RECENTS ***
Tissue damage induces a conserved stress response that initiates quiescent muscle stem cell activation
Cell Stem Cell 2021, by Machado et al.Cardiolipin content controls mitochondrial coupling and energetic efficiency in muscle
Science Advances 2021, by Prola et al.Platelets facilitate the wound-healing capability of mesenchymal stem cells by mitochondrial transfer and metabolic reprogramming
Cell Metabolism 2021, by Levoux et al.From diagnosis to prognosis: Revisiting the meaning of muscle ISG15 overexpression in juvenile inflammatory myopathies
Arthritis Rheumatol 2020, by Hou et al.Distinct phases of postnatal skeletal muscle growth govern the progressive establishment of muscle stem cell quiescence
Stem Cell Reports 2020, by Gattazzo et al.FGFR3 in periosteal cells drives cartilage-to-bone transformation in bone repair
Cell Stem Cell 2020, by Julien et al.X-linked muscular dystrophy in a Labrador Retriever strain: phenotypic and molecular characterisation
Skeletal Muscle 2020, by Barthélémy et al.Notch/CollagenV/CalcR reciprocal signalling retains muscle stem cells in their niche.
Nature 2018, by Baghdadi et al.